- 首页(yè)
- 关于东诚
-
新(xīn)闻中(zhōng)心
- 集团新(xīn)闻
新(xīn)闻中(zhōng)心

-
产(chǎn)业布局
- 原料药业務(wù)板块
- 制剂业務(wù)板块
- 核医(yī)疗业務(wù)板块
- 大健康业務(wù)板块
产(chǎn)业布局

- 创新(xīn)研发
- 人力资源
- 投资者关系
 新(xīn)闻中(zhōng)心
新(xīn)闻中(zhōng)心6月28日,东诚药业集团下属公(gōng)司蓝纳成收到美國(guó)食品药品监督管理(lǐ)局核准签发的关于177Lu-LNC1011注射液的药品临床试验批准通知书,将于近期开展 I 期临床试验。
经查询公(gōng)开资料,目前全球仅有(yǒu)诺华公(gōng)司的同靶点药物(wù) Pluvicto 上市,2023 年 Pluvicto 销售额為(wèi)9.8亿美元,2024 年一季度销售额為(wèi)4.2亿美元。
关于177Lu-LNC1011注射液
01公(gōng)司在研产(chǎn)品177Lu-LNC1011注射液是一种靶向前列腺特异性膜抗原(Prostate Specific Membrane Antigen, 以下简称“PSMA” ) 的放射性體(tǐ)内治疗药物(wù), 拟用(yòng)于治疗 PSMA 阳性表达的晚期前列腺癌患者。
02PSMA是由前列腺上皮细胞分(fēn)泌的一种II型谷氨酸缩肽酶,特异性高表达于前列腺癌及其转移灶的细胞中(zhōng)。177Lu-LNC1011注射液在动物(wù)體(tǐ)内外试验研究中(zhōng)展现出较高的结合亲和力和PSMA靶向特异性,使放射性核素能(néng)够浓聚于肿瘤病灶,实现肿瘤的精(jīng)准治疗。相关的 IIT(investigator-initiated trial,研究者发起的临床研究)研究结果表明受试者耐受性良好,药品安(ān)全性高,在唾液腺中(zhōng)摄取较低,并在肿瘤中(zhōng)实现高吸收剂量。177Lu-LNC1011注射液初步治疗效果显著,有(yǒu)望成為(wèi)一种疗效更好的 PSMA 靶向治疗药物(wù)。
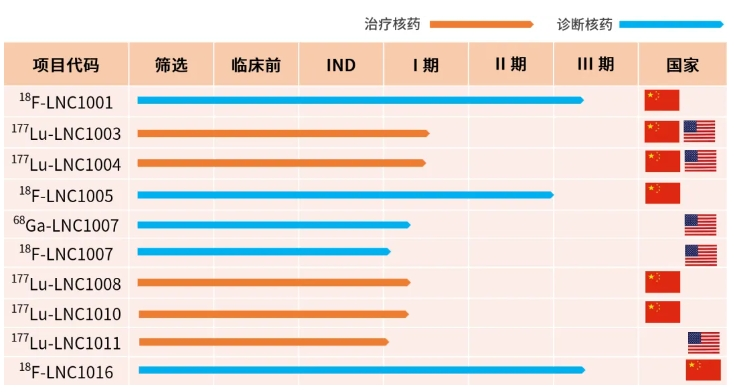
蓝纳成迄今已有(yǒu)涉及4个靶点共10款诊疗一體(tǐ)化创新(xīn)核药,在中(zhōng)美分(fēn)别处于临床试验或IND审评阶段,共计获得15项临床试验批件。5款诊断核药中(zhōng),2款处于III期临床试验,1款处于II期临床试验,2款处于I期临床研究阶段;5款治疗核药处于I期临床研究阶段。
关于蓝纳成
蓝纳成是由东诚药业与國(guó)际顶级分(fēn)子影像及纳米医(yī)學(xué)领域专家陈小(xiǎo)元教授于2021年联合创立的,专注于全球领先的1类诊疗一體(tǐ)化创新(xīn)肿瘤核药研发平台的打造,致力于為(wèi)肿瘤患者提供更加精(jīng)准和有(yǒu)效的治疗方案,推动核医(yī)學(xué)在全球的发展。
(烟台蓝纳成生物(wù)技(jì )术有(yǒu)限公(gōng)司网址:https://www.dc-lnc.com/)


 集团微信公(gōng)众号
集团微信公(gōng)众号
 集团招聘平台
集团招聘平台