- 首页(yè)
- 关于东诚
-
新(xīn)闻中(zhōng)心
- 集团新(xīn)闻
新(xīn)闻中(zhōng)心

-
产(chǎn)业布局
- 原料药业務(wù)板块
- 制剂业務(wù)板块
- 核医(yī)疗业務(wù)板块
- 大健康业務(wù)板块
产(chǎn)业布局

- 创新(xīn)研发
- 人力资源
- 投资者关系
 新(xīn)闻中(zhōng)心
新(xīn)闻中(zhōng)心5月2日,东诚药业集团下属公(gōng)司蓝纳成新(xīn)加坡子公(gōng)司收到美國(guó)食品药品监督管理(lǐ)局核准签发的关于18F-LNC1007注射液的药品临床试验批准通知书,将于近期在澳大利亚开展I期临床试验。
关于18F-LNC1007注射液
01公(gōng)司在研产(chǎn)品18F-LNC1007注射液是一种新(xīn)型双靶点放射性體(tǐ)内诊断药物(wù),同时靶向成纤维细胞活化蛋白(Fibroblast Activation Protein,以下简称“FAP”)和整合素αvβ3 (Integrin αvβ3,以下简称“αvβ3”),拟用(yòng)于诊断FAP和αvβ3阳性的成人实體(tǐ)瘤。
02FAP為(wèi)II型跨膜丝氨酸蛋白酶,高表达于许多(duō)上皮肿瘤相关成纤维细胞(Cancer-Associated Fibroblasts,简称“CAF”)中(zhōng),包括胃癌、食管癌、肺癌、结直肠癌、卵巢癌等,而在正常组织、良性肿瘤间质(zhì)中(zhōng)无表达或表达较低。αvβ3是位于细胞表面的异源二聚體(tǐ)受體(tǐ),在正常血管内皮和上皮细胞很(hěn)少表达,但在肺癌、骨肉瘤、成神经细胞瘤、乳腺癌、前列腺癌、膀胱癌、胶质(zhì)母细胞瘤及浸润性黑色素瘤等多(duō)种实體(tǐ)肿瘤细胞表面有(yǒu)高水平表达, 表明αvβ3在肿瘤生長(cháng)、侵袭和转移过程中(zhōng)起着关键作(zuò)用(yòng)。
03双靶向FAP和αvβ3的18F-LNC1007注射液可(kě)以进一步提高肿瘤的诊断效率,在临床前研究和临床转化研究中(zhōng),18F-LNC1007注射液能(néng)够显著延長(cháng)肿瘤摄取时间、提升肿瘤靶向效率,并具(jù)有(yǒu)良好的肿瘤成像质(zhì)量。有(yǒu)希望在未来成為(wèi)一种非侵入性示踪剂用(yòng)于FAP和/或αvβ3阳性表达患者的临床诊断。
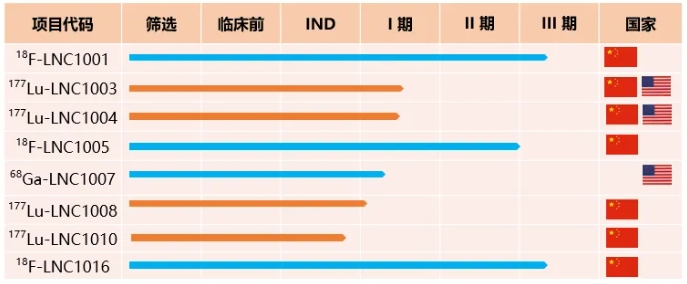
蓝纳成迄今已有(yǒu)涉及4个靶点共9款诊疗一體(tǐ)化创新(xīn)核药,在中(zhōng)美分(fēn)别处于临床试验或IND审评阶段,共计获得13项临床试验批件;5款诊断核药:2款处于III期临床试验,2款处于I期临床研究阶段;4款治疗核药:3款处于I期临床研究阶段,1款处于IND审评阶段。
关于蓝纳成
蓝纳成是由东诚药业与國(guó)际顶级分(fēn)子影像及纳米医(yī)學(xué)领域专家陈小(xiǎo)元教授于2021年联合创立的,专注于全球领先的1类诊疗一體(tǐ)化创新(xīn)肿瘤核药研发平台的打造,致力于為(wèi)肿瘤患者提供更加精(jīng)准和有(yǒu)效的治疗方案,推动核医(yī)學(xué)在全球的发展。(烟台蓝纳成生物(wù)技(jì )术有(yǒu)限公(gōng)司网址:https://www.dc-lnc.com/)


 集团微信公(gōng)众号
集团微信公(gōng)众号
 集团招聘平台
集团招聘平台